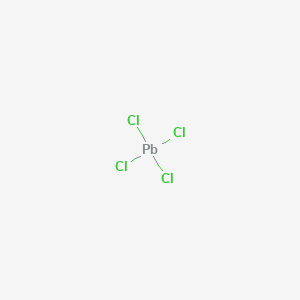
Cloruro de plomo (IV) — un compuesto inorgánico binario, sal del metal plomo y ácido clorhídrico con la fórmula PbCl4, un líquido aceitoso amarillo, reacciona con el agua.
Obtención
- Descomposición en frío en ácido sulfúrico concentrado de ácido hexacloroplúmbico o su sal:
-
- H2[PbCl6] →0oC PbCl4 + 2 HCl
- (NH4)2[PbCl6] + H2SO4 →0oC PbCl4 + (NH4)2SO4 + 2 HCl
- Acción de cloruro de hidrógeno sobre óxido de plomo:
-
- PbO2 + 4 HCl → PbCl4 + 2 H2O
Propiedades físicas
El cloruro de plomo (IV) — es un líquido aceitoso amarillo, reacciona con el agua, a 100°C se descompone con explosión.
Propiedades químicas
- Al calentarse se descompone (puede ser con explosión):
-
- PbCl4 →30−100oC PbCl2 + Cl2
- Se hidroliza con agua:
-
- PbCl4 + 2 H2O → PbO2 + 4 HCl
- Se disuelve en ácido clorhídrico concentrado:
-
- PbCl4 + 2 HCl → H2[PbCl6]
- Se descompone con álcalis:
- PbCl4 + 4 NaOH → PbO2 ↓ + 4 NaCl + 2 H2O
- PbCl4 + 6 NaOH → Na2[Pb(OH)6] + 4 NaCl
| Cloruro de plomo (IV) | |
|---|---|
 |
|
| Nombre sistemático | Cloruro de plomo |
| Nombres tradicionales | Cuatro cloruros de plomo |
| Fórmula química | PbCl4 |
| Fórmula semidesarrollada | PbCl4 |
| Estado de agregación | líquido aceitoso amarillo |
| Masa molar | 349,01 g/mol |
| Densidad | 3,18 g/cm³ |
| Temperatura | |
| fusión | -7 °C |
| ebullición | explosión. 105 °C |
| Entalpía | |
| de formación | -328,9 kJ/mol |
| Número CAS | 13463-30-4 |
| PubChem | 123310 |
| SMILES |
Cl[Pb](Cl)(Cl)Cl
|
| InChI |
1S/4ClH.Pb/h4*1H;/q;;;;+4/p-4
PJYXVICYYHGLSW-UHFFFAOYSA-J
|
| ChemSpider | 109913 |
| Datos para condiciones estándar (25 °C, 100 kPa), salvo indicación contraria. | |