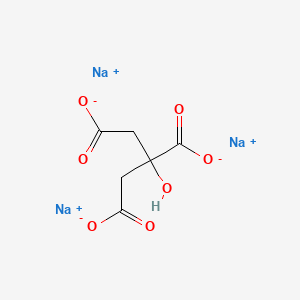
citrato de sodio (лат. Natrii citras) — sal sódica del ácido cítrico Na3C6H5O7. El citrato de sodio tiene un sabor salado-ácido moderadamente pronunciado. Debido a esta característica de los citratos de elementos alcalinos y alcalinotérreos (por ejemplo, citratos de sodio y calcio), se les conoce como «sales ácidas» (a veces, el ácido cítrico también se denomina erróneamente así). El citrato de sodio se utiliza principalmente como especia (condimento), que aporta un sabor especial, o como conservante (aditivo alimentario E331).
Ámbitos de aplicación
- Como aditivo aromatizante, forma parte de muchas bebidas carbonatadas con sabor a limón o lima, así como de bebidas energéticas.
- El citrato puede utilizarse como compuesto tampón, previniendo cambios en el pH.
- Se utiliza para controlar la acidez de algunos platos, como los postres de gelatina.
- Es una sal fundente utilizada en la producción de queso procesado desde su invención en 1911.
- Se utiliza para regular la acidez en las máquinas de café.
- El citrato de sodio se forma al disolver en agua muchos «medicamentos de disolución rápida», como (antiácidos — para la acidez estomacal).
- Se utiliza para reducir las molestias en infecciones del sistema urogenital, como la cistitis; reduce la acidez en acidosis renales periféricas y también se emplea como regulador osmótico (laxante).
- En forma de solución, es uno de los componentes del medio para la descongelación de semen animal en la inseminación artificial.
- En forma de solución al 5 %, se utiliza para determinar la velocidad de sedimentación globular (VSG) mediante el método de Panchenkov.
- Se utiliza en química analítica como componente para la determinación de iones amonio.
- En forma de solución al 4 %, se utiliza como anticoagulante en la donación de componentes sanguíneos por aféresis.
- Puede utilizarse en líquidos limpiaparabrisas.
- Es uno de los componentes en medicamentos para la deshidratación.
- Se utiliza como retardador en morteros de yeso-cemento para la cementación de pozos.

Historia del citrato de sodio
En 1914, el médico belga Albert Hustin y el físico-investigador argentino Luis Agote utilizaron con éxito el citrato de sodio como anticoagulante en las transfusiones de sangre. Todavía se utiliza en medicina para la toma de muestras de sangre y en los bancos de sangre (para transfusiones). El ion citrato forma complejos con el calcio en la sangre, interrumpiendo así el proceso de coagulación sanguínea.
En 2003, Oöpik (V. Oöpik) y otros demostraron que la ingesta de citrato de sodio en una cantidad de aproximadamente 37 gramos mejora el resultado en una carrera de 5 kilómetros en 30 segundos.


Metabolización en el organismo humano
En el organismo humano, el citrato de sodio y el ácido cítrico existen principalmente en forma de ion citrato. El ion citrato es uno de los metabolitos del ciclo de los ácidos tricarboxílicos, formándose por la unión de oxalacetato y acetil-CoA bajo la acción de la enzima citrato sintasa en la matriz mitocondrial. Este proceso permite que el acetil-CoA entre en el ciclo del citrato, donde se utiliza para la producción de energía. La cantidad de citrato en las mitocondrias puede variar en función del gasto energético del organismo y de sus órganos individuales, así como del estado funcional de las células individuales. Así, en condiciones de ayuno, en los hepatocitos, la mayor parte del oxalacetato está ocupada en la gluconeogénesis y la cantidad de citrato formado se reduce drásticamente.
Asimismo, el ion citrato participa en el transporte indirecto de acetil-CoA desde las mitocondrias al citoplasma para las necesidades de síntesis, por ejemplo, de ácidos grasos. En este proceso, el citrato se transfiere de la matriz mitocondrial al citoplasma, donde, bajo la acción de la enzima ATP-citrato liasa, se escinde en acetil-CoA y oxalacetato. Cabe señalar que dicho transporte solo se produce en caso de exceso de citrato en las mitocondrias, es decir, cuando la célula está completamente provista de energía, y no tiene lugar en caso de su deficiencia. De este modo, se asegura una regulación indirecta del transporte de acetil-CoA y la síntesis de ácidos grasos desde las mitocondrias, dependiendo del estado funcional de las células.

| Citrato de sodio | |
|---|---|
 |
|
| Fórmula química | Na3C6H5O7 |
| Estado de agregación | polvo cristalino blanco |
| Masa molar | 258,07 g/mol |
| Densidad | 1,7 g/cm³ |
| Temperatura | |
| fusión | 310 °C |
| ГОСТ | ГОСТ 31227-2013 ГОСТ 31227-2004 |
| Número CAS | 68-04-2 |
| PubChem | 6224 |
| Número EINECS | 200-675-3 |
| SMILES |
[Na+].[Na+].[Na+]. O=C([O-])CC(O)
(CC(=O)[O-])C([O-])=O |
| InChI |
1S/C6H8O7.3Na/c7-3(8)1-6(13,5(11)12)2-4(9)10;;;/h13H,1-2H2,(H,7,8)(H,9,10)(H,11,12);;;/q;3*+1/p-3
HRXKRNGNAMMEHJ-UHFFFAOYSA-K
|
| Código Alimentarius | E331iii |
| RTECS | GE8300000 |
| ChEBI | 53258 |
| ChemSpider | 5989 |
| Datos para condiciones estándar (25 °C, 100 кПа), salvo indicación contraria. | |