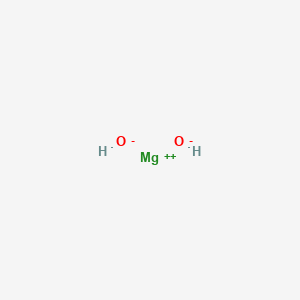Hidróxido de magnesio — sustancia inorgánica, hidróxido básico del metal magnesio, tiene la fórmula Mg(OH)2. Una base débil y poco soluble.
Descripción
En condiciones estándar, el hidróxido de magnesio es una sustancia amorfa. A temperaturas superiores a 350 °C, se descompone en óxido de magnesio y agua. Absorbe dióxido de carbono y agua del aire, formando carbonato básico de magnesio. El hidróxido de magnesio es prácticamente insoluble en agua, pero soluble en sales de amonio. Es una base débil; incluso una pequeña parte de ella disuelta en agua confiere a la solución una reacción ligeramente alcalina y tiñe los indicadores, por ejemplo, la fenolftaleína, de color rosa. Se encuentra en la naturaleza en forma del mineral brucita.
Obtención
- Reacción de sales de magnesio solubles con álcalis:
- En forma general:
Mg2+ + 2 OH− ⟶ Mg(OH)2 ↓
- Ejemplos:
MgCl2 + 2 NaOH ⟶ Mg(OH)2 ↓ + 2 NaCl
Mg(NO3)2 + 2 KOH ⟶ Mg(OH)2 ↓ + 2 KNO3
- Reacción de una solución de cloruro de magnesio con dolomita calcinada:
MgCl2 + CaO ⋅ MgO + 2 H2O ⟶ 2 Mg(OH)2 ↓ + CaCl2
- Reacción de magnesio metálico con vapor de agua:
Mg + 2 H2O ⟶ Mg(OH)2 ↓ + H2 ↑
Propiedades químicas
- Como todas las bases débiles, el hidróxido de magnesio es térmicamente inestable. Se descompone al calentarse hasta 350 °C:
Mg(OH)2 →ΔT MgO + H2O
- Reacciona con ácidos para formar sal y agua (reacción de neutralización):
Mg(OH)2 + 2 HCl ⟶ MgCl2 + 2 H2O
Mg(OH)2 + H2SO4 ⟶ MgSO4 + 2 H2O
- Reacción con óxidos ácidos para formar sal y agua:
Mg(OH)2 + SO3 ⟶ MgSO4 + H2O
- Reacción con soluciones concentradas calientes de álcalis para formar hidroxomagnesatos:
Mg(OH)2 + 2 NaOH ⟶ Na2[Mg(OH)4]
Mg(OH)2 + Sr(OH)2 ⟶ Sr[Mg(OH)4]

Aplicaciones
El hidróxido de magnesio se utiliza para la fijación de dióxido de azufre, como floculante para el tratamiento de aguas residuales, como retardante de llama en polímeros termoplásticos (poliolefinas, PVC), como aditivo en detergentes, para la obtención de óxido de magnesio, la refinación de azúcar, y como componente de pastas dentales.
En medicina, se utiliza como medicamento para neutralizar el ácido en el estómago, y también como un laxante muy potente.
En la Unión Europea, el hidróxido de magnesio está registrado como aditivo alimentario E528.
| Hidróxido de Magnesio | |
|---|---|
| Nombre sistemático | Hidróxido de Magnesio |
| Fórmula química | Mg(OH)2 |
| Fórmula semidesarrollada | Mg(OH)2 |
| Estado de agregación | sólido |
| Masa molar | 58.35 g/mol |
| Densidad | 2,3446 (20 °C) |
| Temperatura | |
| de fusión | 350 °C |
| de inflamabilidad | no inflamable °C |
| Entalpía | |
| de formación | –925 kJ/mol |
| Solubilidad | |
| en agua | 0,0012 g/100 ml |
| Índice de refracción | 1.559 |
| Estructura cristalina | trigonal |
| Número de registro CAS | 1309-42-8 |
| PubChem | 73981 |
| Número de registro EINECS | 215-170-3 |
| SMILES |
[OH-].[Mg+2].[OH-]
|
| InChI |
1S/Mg.2H2O/h;2*1H2/q+2;;/p-2
VTHJTEIRLNZDEV-UHFFFAOYSA-L
|
| Código Alimentarius | E528 |
| RTECS | OM3570000 |
| ChEBI | 6637 |
| ChemSpider | 14107 y 21169899 |
| Datos para condiciones estándar (25 °C, 100 kPa), salvo indicación contraria. | |